A continuación podéis descargar un artículo divulgativo preparado en el Prácticum celebrado en la Clínica Universitaria de Visión Integral de Murcia para el Máster en Rehabilitación Visual de la Universidad de Valladolid.
A continuación podéis descargar un artículo divulgativo preparado en el Prácticum celebrado en la Clínica Universitaria de Visión Integral de Murcia para el Máster en Rehabilitación Visual de la Universidad de Valladolid.

El Instituto Ramón Castroviejo de la Universidad Complutense de Madrid acogió la segunda reunión para la puesta en marcha del Observatorio Nacional de Enfermedades Raras Oculares (ONERO) El pasado lunes 22 de enero. En esta reunión se dieron cita 17 asociaciones de toda España y otras que no pudieron acudir estuvieron presentes mediante el voto delegado. El Dr. José Carlos Pastor de la Universidad de Valladolid y Manuel Posadas, director del Registro de Enfermedades Raras del Instituto de Salud Carlos III también participaron en esta reunión. Además, la ONCE a través de su vicepresidenta Patricia Sanz y FEDER con la intervención de su asesor jurídico Fernando Torquemada también mostraron su apoyo al proyecto.
Por James Gallagher
El NHS pagará por 10 pacientes ciegos para que puedan tener "ojos biónicos" y ayudarles a tratar una forma heredada de la ceguera.
El ojo biónico es un implante de retina que interpreta las imágenes captadas por una cámara de video en miniatura que se usa en un par de gafas.
Cinco pacientes serán tratados en el Hospital Real de ojos de Manchester y cinco en el Hospital Moorfields Eye en 2017.
Ellos serán supervisados un año más tarde para ver cómo se adaptan en la vida cotidiana.
"Estoy muy contento", dijo el profesor Paulo Stanga del hospital de Manchester.
Ha estado involucrado en los ensayos anteriores del Argus II Ojo biónico, hechos por la compañía Second Sight, en la retinitis pigmentosa.
Y agregó: "Se superaron todas nuestras expectativas cuando nos dimos cuenta de que uno de los pacientes con retinitis pigmentosa utilizando el ojo biónico podía identificar letras grandes por primera vez en su vida adulta."
Esta enfermedad, que a menudo se pasa de padres a hijos, destruye las células sensibles a la luz en la retina. Conduce a la pérdida de la visión y, finalmente, la ceguera.
Luces parpadeantes
Keith Hayman, que tiene 68 años y es de Lancashire, fue equipado con el ojo biónico en Manchester.
Se vio obligado a retirarse de su antigua carnicería antes de tiempo debido a la enfermedad y había sido ciego desde hace más de dos décadas.
Él dijo: "Después de haber pasado la mitad de mi vida en la oscuridad, ahora puedo decir cuando mis nietos corren hacia mí y ver las luces parpadeantes en los árboles de Navidad.
"Estar hablando con un amigo, que podría haberse alejado y no lo notaba y seguía hablando solo, esto ya no ocurre más, porque yo puedo saber cuando se han ido.
"Estas pequeñas cosas marcan la diferencia para mí."
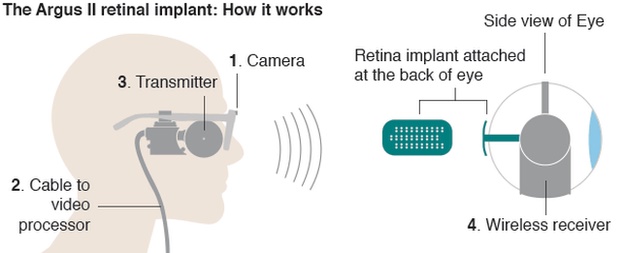
Cómo funciona
El implante del ojo biónico recibe la información visual de una cámara en miniatura montada en unas gafas que lleva el paciente.
Las imágenes se convierten en impulsos eléctricos y se transmiten de forma inalámbrica a una serie de electrodos colocados en la retina.
Los electrodos estimulan las células restantes de la retina que envían la información al cerebro.
Gregoire Cosendai, dice: "Esta es la primera vez en la historia que cualquier tratamiento para este tipo de ceguera ha existido y ahora se va a ofrecer gratuitamente a los pacientes ciegos.”
"Esta es una gran victoria para las personas ciegas en el Reino Unido que nos han apoyado en nuestra misión de seis años para financiar Argus II en Inglaterra."
Dr Jonathan Fielden, desde el NHS de Inglaterra, dijo: "Este procedimiento altamente innovador financiado por el NHS muestra una promesa real y podría cambiar la vida.”
"El NHS ha implantado las innovaciones médicas mundiales que van desde la cirugía de catarata moderna, nuevas vacunas y las prótesis de cadera, ahora, una vez que el NHS está a la vanguardia del aprovechamiento de la ciencia de vanguardia para el beneficio de los pacientes en este país."
Ocugen Inc., una biotecnología con sede en Aurora de investigación de enfermedades de los ojos, dijo que ha recaudado 6 millones de dólares en financiación.
Ocugen fue co-fundada por Shankar Musunuri y Uday Kompella , que es un profesor de la Universidad de Colorado Anschutz Medical Campus , donde tiene su sede la empresa.
La biotecnología está avanzando la investigación de fármacos para tratar la retinitis pigmentosa (OCU100), degeneración macular (OCU200) e injerto contra huésped ocular (OCU300).
"Con estos fondos, continuaremos nuestros esfuerzos para promover agresivamente el programa OCU300 hacia una presentación IND (nuevo fármaco en investigación) dentro de un año, con lo que esta terapia muy necesaria estará más cerca de los pacientes que lo necesitan", dijo Musunuri, que también es el CEO y presidente de la biotecnología, en un comunicado.
La sede de la empresa se encuentran en Bioscience Park Center, 12635 E Montview Blvd. en Aurora y también hay una oficina en Malvern, Pennsylvania.
Rodrigo Lanzón.
Vocal de Investigación,
Spark Therapeutics proporcionará, a los médicos y los pacientes elegibles, acceder a las pruebas genéticas y a un asesoramiento a más de 30 genes relacionados con ciertas formas de enfermedades retinianas hereditarias (IRD), un grupo de enfermedades de los ojos que se cree que afecta a más de 100.000 personas en los Estados Unidos. El identificar su enfermedad retiniana hereditaria, o su ID IRD, la iniciativa se dio a conocer oficialmente esta semana en la Academia Americana de Oftalmología (AAO) 2016 Reunión Anual de Spark Therapeutics, una empresa totalmente integrada en la terapia génica que busca transformar las vidas de los pacientes con enfermedades debilitantes a través de tratamientos científicos de una sola aplicación.
"Confirmar el diagnóstico genético es una puerta de entrada fundamental para los pacientes con enfermedades hereditarias de retina y esta iniciativa ayudará a los pacientes, cuidadores y a la comunidad médica entender mejor su enfermedad," dijo Mark Pennesi, MD, Ph.D., profesor asociado de oftalmología en el OHSU Facultad de Medicina de OHSU Casey Eye Institute. "Las pruebas genéticas pueden proporcionar información valiosa sobre la causa subyacente del trastorno de la visión y que los pacientes puedan conectarse a otras personas que viven con la misma condición. Con la identificación de nuevos genes y el creciente énfasis en la investigación en terapia génica, nuestra comprensión de los IRD está cambiando rápidamente. Las personas con IRD se animan a someterse a la prueba incluso si previamente han sido probados para una enfermedad genética ".
La iniciativa fue desarrollada en respuesta a la retroalimentación de los defensores, las familias afectadas por el IRD y profesionales de la salud acerca de las actuales barreras que impiden el acceso a la configuración genética de los IRD de una manera coherente y simplificado. Spark Therapeutics está trabajando con los médicos de todo el país que estarán equipados para facilitar las pruebas genéticas IRD para los pacientes elegibles. La elegibilidad será determinada por el médico del paciente. Los médicos participantes enviarán muestras de prueba a un laboratorio independiente, que procesará la muestra y entregará los resultados de las pruebas que puedan confirmar la mutación genética específica que causa la I RD. Esta información puede ayudar a determinar el mejor curso de acción para el paciente. Los pacientes elegibles recibirán la prueba genética ofrecida por ID IRD libre de cargo, sujeto a los términos y condiciones de la iniciativa. La iniciativa también dispone de conexión opcional a consejeros genéticos independientes sin coste alguno para los participantes de los pacientes elegibles.
"Esta iniciativa de proyección gratuita ofrecida por Spark da a los pacientes elegibles y sus médicos fácil acceso a las pruebas de laboratorio durante más de 30 genes causantes de enfermedades," dijo Steve Rose, jefe de investigación de la Fundación para la Lucha contra la Ceguera. "Si bien la decisión de hacerse la prueba es siempre una decisión personal entre los pacientes y sus médicos, este tipo de información puede identificar la causa genética subyacente de la enfermedad de la retina de una persona y ayudarles a entender cómo la enfermedad puede afectar a la visión durante su vida. Además, esta iniciativa proporcionará más datos sobre la prevalencia de ciertas mutaciones genéticas, lo que podría ayudar a orientar nuevas investigaciones ".
Spark Therapeutics ha estado trabajando estrechamente con los médicos en los Estados Unidos y en otros países de todo el mundo para ayudar a proporcionar acceso a la detección genética para las personas con IRD. Esfuerzos similares están en marcha o en desarrollo a través de América del Sur y Europa. Se estima que más de 2 millones de personas viven con IRD a nivel mundial, pero sólo un pequeño porcentaje de ellos han sido seleccionados genéticamente debido al acceso limitado a la información y sobre las pruebas genéticas.
"Estamos orgullosos de lanzar esta iniciativa nacional importante para las personas con IRD para apoyar la adopción de la comunidad médica de diagnósticos precisos de base genética", dijo Jeffrey D. Marrazzo, director general de Spark. "Como líder en el desarrollo de terapias génicas en investigación de los IRD, tenemos una responsabilidad para ayudar a proporcionar a los pacientes, cuidadores y profesionales de la salud un acceso a la información genética necesaria para tomar las decisiones."
Spark está coordinando con otras dos empresas independientes para ofrecer este servicio. PreventionGenetics, y Laboratory Improvement Amendments (CLIA) - y la Organización Internacional para la Estandarización (ISO) de laboratorio 15189-acreditado como uno de los más grandes y más completos de todos los laboratorios en los Estados Unidos, llevará a cabo las pruebas ya sea de sangre o muestras de saliva recogidas a través de un kit de prueba proporcionada a los médicos participantes. lnformedDNA, la mayor red de los proveedores independientes de la nación de los especialistas en genética, proporcionará servicios de asesoramiento genético a pacientes, cuidadores y profesionales de la salud a través del proceso, y ayudará a discutir la interpretación de los resultados de las pruebas.
Las personas que viven con el IRD o sus familiares pueden iniciar el proceso para determinar la elegibilidad papa hablar con su profesional de la salud acerca de Identificación SU IRD o visitando www.idyourird.com . El sitio incluye un breve screener del paciente, términos y condiciones completos de la iniciativa, y otros recursos. Información de la enfermedad adicional, incluyendo una guía para ayudar a las familias a trabajar con los profesionales de la salud para buscar un diagnóstico genético, se puede encontrar en www.asharedvision.com . Spark Terapéutica ID SUS enlaces IRD también están disponibles en 1-855- SPARKTX (1-855-772-7589)
Rodrigo Lanzón.
Vocal de Investigación,
07 Abr el año 2016 por Emily McCormick
Una prótesis de retina que podrían restaurar la visión de pacientes con retinitis pigmentosa (RP) ha dado un gran paso hacia adelante en su intento de estar disponible a través del NHS en Inglaterra.
Los desarrolladores y los fabricantes del dispositivo Argus II, Second Sight, confirmaron que ayer (6 de abril) NHS Inglaterra publicó una consulta pública sobre la financiación del NHS del dispositivo.
La consulta se ha emitido siguiendo las recomendaciones positivas para el dispositivo por profesionales de la salud que aconsejan a la autoridad sanitaria financiación del gobierno del Reino Unido para servicios especializados en Inglaterra.
Se pide a las partes interesadas, como los pacientes anteriores Argus II y los que podrían beneficiarse del dispositivo en el futuro, las organizaciones benéficas y los médicos, para compartir sus puntos de vista sobre un nuevo proyecto de política para el tratamiento con el ojo biónico a través del NHS.
La política se ha elaborado tras una investigación realizada por el Grupo Clínico de Oftalmología Servicios Especializados, que reportó resultados positivos en relación con el Argus II sobre la eficacia, la seguridad, la califica de beneficios de vida y relación coste-eficacia.
El proyecto de política recomienda que el dispositivo está financiado por la puesta en marcha a través del programa de Evaluación (CTE), que generalmente se recomienda cuando NHS de Inglaterra cree que un tratamiento puede ofrecer beneficios clínicos, pero quiere recoger más pruebas, un portavoz de Second Sight explicó.
La consulta permanecerá abierta durante 30 días, después de lo cual se revisará el borrador de la política.
El dispositivo ya está accesible en muchas partes de Europa, así como los EE.UU...
Comentando el lanzamiento de la consulta, Second Sight Medical Products vicepresidente de Europa, Grégoire Cosendai, dijo: "Second Sight está encantada con este desarrollo muy positivo. Este es un momento crucial en nuestra misión de seis años para hacer Argus II disponible en el NHS en Inglaterra.
"La contribución de los pacientes y cirujanos ingleses fue clave para nuestro éxito en tener el Argus II aprobado y financiado en otras partes de Europa y en los EE.UU. Apoyamos plenamente el programa CTE, y esperamos con interés trabajar con el NHS en esta iniciativa para cambiar RP pacientes en el Reino Unido la vida. "
La bienvenida a la consulta, el cirujano consultor de retina en el Hospital Moorfields Eye, Lyndon da Cruz, dijo: "Como un cirujano que ha puesto a prueba este tratamiento, he visto de primera mano los resultados positivos que puede tener para los pacientes. Si se pone a disposición el tratamiento en el NHS en Inglaterra, que traerá esperanza a los muchos pacientes con pérdida de la visión profunda de RP, que podrían experimentar lo real, y, en algunos casos, un cambio de vida, beneficios de la prótesis. ".